Ahmet T. Turgut, MD, Erkan Kismali, MD, Vikram S. Dogra, MD
Трансректальное ультразвуковое исследование (ТРУЗИ) традиционно рассматривается как ключевой тест для изображения предстательной железы, которое обеспечивает клинически важной информацией при доброкачественных и злокачественных поражениях, в том числе доброкачественной гиперплазии предстательной железы (ДГПЖ), простатите, обструктивном бесплодии и раке предстательной железы (РПЖ). На сегодняшний день основными причинами для направления пациентов на ТРУЗИ являются выявление и оценка РПЖ и ультразвуковое наведение при биопсии предстательной железы.
В зрелом возрасте нормальная предстательная железа имеет средние размеры от 4,0 до 4,5 см, от 2,5 см до 3,0 и от 3,0 до 4,0 см в поперечном, передне-заднем и кранио-каудальном направлениях, соответственно. Эта железа окутана тонкой псевдокапсулой, которую вряд ли можно отличить от окружающих фасциальных плоскостей. Анатомически сосудисто-нервные пучки, которые перфорируют капсулу предстательной железы имеют решающее значение, потому что они являются основным местом слабости капсульного аппарата и потенциально склонны к вовлечению в опухолевый процесс. Картина нормальной железы при ТРУЗИ зависит от возраста. У молодых мужчин гиперплазия железистой ткани является незначительной, в то время как у мужчин в возрасте предстательная железа превращается в большую железу с более округлой формой из-за развития ДГПЖ.
В среднем 70% нормальной предстательной железы состоит из железистых элементов, а оставшиеся 30% - состоят из фиброзно-мышечной стромы. Железистая ткань предстательной железы обычно состоит из внутренних желез, которые включают переходную зону и околомочеточниковую железистую ткань и внешних желез, которые занимают периферическую и центральную зоны. ТРУЗИ, как правило, позволяет отличить переходную зону, которая расположена спереди, как гипоэхогенная область, от периферической зоны, которая является эхогенной и однородной по своей эхотекстуре, по сравнению с остальной частью железы. Центральная зона, с другой стороны, едва отличается от периферической зоны у здоровых взрослых мужчин. Переходная зона является основным местом для гиперпластических изменений, составляет большую часть в пропорциональном соотношении ткани предстательной железы у пожилых мужчин, и может дополнительно быть местом развития РПЖ, приблизительно в 20%. Следует отметить, что от 1% до 5% РПЖ расположено в центральной зоне. Периферическая зона, будучи также основным местом развития хронического простатита, приводит примерно к 70% РПЖ. Раковое поражение в переходной зоне, с другой стороны, вряд ли можно отличить от узелков при ДГПЖ по данным ТРУЗИ.
На сегодня биплановые датчики в сочетании с концевыми и боковыми датчиками позволяют получать мультиплановые изображения в полукоронарной, осевой, сагиттальной проекциях при трансректальном сканировании предстательной железы. Технически, датчики с частотой от 5 до 8 МГц обеспечивают более высокое разрешение для периферической части железы, что имеет решающее значение для точности выбора образцов в ходе процедуры биопсии. Воздушные пузырьки - артефакты оказывают негативное влияние на качество изображения, что можно избежать с помощью ультразвукового геля, который наносится на латексный презерватив, надетый на датчик. Самостоятельный прием клизмы накануне процедуры помогает в эвакуации газа и кала, а это еще один фактор, который может привести к искажению изображения при ТРУЗИ. Сопутствующее пальцевое ректальное исследование может быть полезным для выявления подозрительных находок при физикальном обследовании, которые коррелируют с аномалиями при ТРУЗИ. Большинство экспертов предпочитают положение пациента лежа на левом боку, потому что оно хорошо переносится. В заключение, полный мочевой пузырь обеспечивает чистое поле зрения с основой предстательной железы, что помогает в ее лучшей визуализации. Тем не менее, по наблюдению авторов, клиническая практика такова, что мочевой пузырь не должен быть слишком растянутым, поскольку это может привести к возникновению недержания мочи во время сопутствующей процедуры биопсии.
ТРУЗИ оценка предстательной железы начинается с системного сканирования в поперечной или полукоронарной плоскости, начиная от уровня семенных пузырьков, которые прилегают к основанию предстательной железы, и продолжая вниз до апикального уровня с визуализацией железистых зон. Затем проводится сканирование в сагиттальной плоскости для выявления любой долевой асимметрии, а также и для подтверждения подозрительных образований, обнаруженных при осевом или коронарном сканировании. Простатические и экстрапростатические структуры, которые оцениваются при системном подходе, перечислены в таблице 1. Важно отметить, что формула эллипсоида позволяет вычислить объем предстательной железы с помощью диаметров по ортогональным осям:
Объем предстательной железы = 0.52 х td х apd x ccd
где td, apd и ccd представляют поперечный, передне-задний и кранио-каудальный диаметры предстательной железы, соответственно.
Анатомические структуры, которые оцениваются при ТРУЗИ
У больных с диагнозом РПЖ, оценка объема предстательной железы может быть необходима для проведения соответствующей терапии. Соответствующая оценка может быть также эффективна при лечении пациентов, которым не выставлен диагноз рака, так как это может помочь в проведении прямой терапии пациентам при лечении симптомов обструкции нижних мочевыводящих путей. Трансректальный ультразвуковой подход к предстательной железе также позволяет оператору выполнять различные диагностические и терапевтические вмешательства при РПЖ, благодаря значительно более высокому разрешению, по сравнению с другими методиками ультразвукового сканирования.
РПЖ является второй ведущей причиной развития рака, связанной со смертностью у мужчин. Помимо того, что это заболевание относится к разряду основных медицинских проблем, это также важный вопрос общественного здравоохранения, так как оно приводит к значительным экономическим затратам. Хотя раннее выявление заболевания важно для адекватного лечения, незначительные очаги рака также могут быть обнаружены в дополнение к значительному опухолевому поражению. На сегодняшний день основными инструментами, используемыми для диагностики заболевания являются: пальцевое ректальное исследование, сывороточные уровни простат-специфического антигена (ПСА) и биопсия предстательной железы под ТРУЗИ контролем. В настоящее время положительная прогностическая ценность биопсии предстательной железы на основе пальцевого ректального исследования, ПСА и выводов ТРУЗИ низкая, и это приводит к значительному количеству ненужных биопсий. Следовательно, улучшение точности диагностических методов исследования РПЖ является очевидной необходимостью.
Наиболее частым показанием для ТРУЗИ исследования предстательной железы является диагностическая оценка при подозрении на РПЖ. По-видимому, раннее выявление РПЖ тесно связано со снижением смертности, так как выявление на ранней стадии заболевания является, зачастую, единственным шансом для излечения. До широкого внедрения диагностических средств, позволяющих выявлять заболевания на ранних стадиях, таких как: пальцевое ректальное исследование, ТРУЗИ и определение уровня ПСА, РПЖ часто диагностировался в поздней стадии, в результате чего пациенты умирали в более короткие сроки. Хотя сывороточный уровень общего ПСА (ОПСА) более 4 нг/мл может подразумевать наличие РПЖ, пациенты с ДГПЖ и воспалительными расстройствами предстательной железы также могут иметь повышенный сывороточный уровень общего ПСА. Отсутствие специфичности сывороточного уровня общего ПСА для скрининга РПЖ неизбежно привело к дальнейшим усилиям, направленным на определение идеального протокола, который бы объединял ПСА, ТРУЗИ и пальцевое ректальное исследование для улучшения специфичности без снижения чувствительности. Несмотря на то, что ТРУЗИ признается лучшим методом для ультразвукового наведения при биопсии, его низкая положительная прогностическая ценность в диагностике злокачественных новообразований рассматривается как существенный недостаток.
С момента своего первого клинического внедрения в 60-х годах, достигнуто стойкое улучшение технологии ТРУЗИ. Хотя существует консенсус в отношении использования ТРУЗИ для оценки размера предстательной железы и ультразвукового наведения при биопсии, его ограниченная ценность для точного обнаружения начальной стадии РПЖ и определения локального опухолевого распространения по-прежнему представляет большой клинический вопрос об эффективности его использования. Тем не менее, серошкальное ультразвуковое исследование позволяет четко выделить зональную анатомию предстательной железы, при этом железа может быть легко очерчена при ТРУЗИ от перипростатических тканей, в том числе прямой кишки, сосудисто-нервных пучков и жировой ткани.
Классически, гипоэхогенное поражение в периферической зоне может представлять собой злокачественный процесс, хотя РПЖ может реже иметь изоэхогенные или гиперэхогенные характеристики (рис. 1 и 2А).

Рис. 1. Рак предстательной железы. Изображение в поперечной проекции серошкального ТРУЗИ, которое показывает нечетко определенное, слегка гипоэхогенное образование в субкапсулярной зоне левой доли (стрелка), которое было гистологически верифицировано как аденокарцинома.

Рис. 2. Рак предстательной железы. (А) Изображение в поперечной проекции серошкального ТРУЗИ без четкого поражения в периферической зоне. (В) Изображение в поперечной проекции цветного допплеровского ТРУЗИ того же больного, показывает область повышенной васкуляризации в правой периферической зоне (стрелка), что стало единственным признаком гистопатологически выявленной аденокарциномы. Опухоль не была видна при серошкальном ТРУЗИ из-за ее изоэхогенной природы.
В настоящее время требуется применение других, менее специфических особенностей для диагностики РПЖ, потому что значительная часть выявляемого РПЖ - изоэхогенная. В связи c этим могут быть полезными характеристики: асимметрия, эхотекстура или железистый край. Соответственно этому, неспецифический неравномерный эхосигнал, или выпуклость, или прерывистый контур капсулы может подразумевать наличие РПЖ. Однако, около половины поражений при РПЖ невидимы при серошкальном ультразвуковом исследовании. Более того, некоторые виды патологии, такие как: ДГПЖ, простатит, атрофия, гематома, эктазия протоков и интраэпителиальная неоплазия могут имитировать картину РПЖ при серошкальном ультразвуковом исследовании. Еще одной проблемой для оценки РПЖ является то, что он в основном мультифокальный; одиночное округлое образование также может иметь место, но такая картина встречается реже. Морфологически, только 30% РПЖ может проявляться в качестве одиночного узелка (рис. 3А), в то время как поражение, которое сопровождается инфильтративным компонентом, встречается примерно у 50% пациентов (рис. 4А, В), а инфильтративная картина преобладает в остальных 20% . Ультразвуковая картина наводит на мысль о распространенном РПЖ при диффузно гипоэхогенной и гетерогенной эхотекстуре периферической зоны, которая либо изоэхогенная, либо гиперэхогенная по сравнению с внутренней железистой тканью нормальной предстательной железы (рис. 5А).

Рис. 3. Рак предстательной железы. (А) Изображение в поперечной проекции серошкального ТРУЗИ показывает округлое, гипоэхогенное образование, которое расположено в правой периферической зоне (стрелка). Ни цветное (B), ни энергетическое (С) допплеровское ТРУЗИ не выявило заметного увеличения кровотока, который бы прогнозировал неоваскуляризацию, характерную для РПЖ. (D) Поперечное ТРУЗИ изображение отражает траекторию иглы, которая используется для отбора проб при биопсии вышеупомянутого поражения.
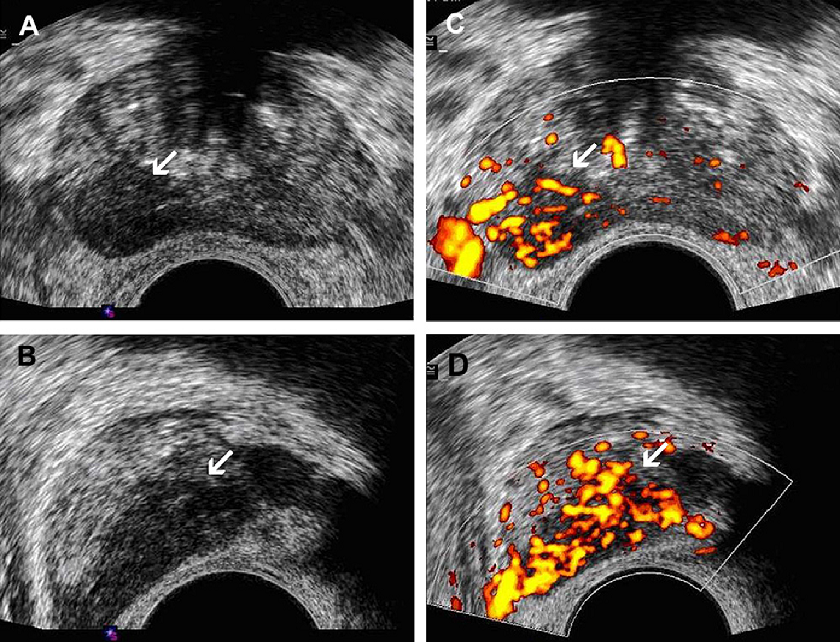
Рис. 4. Рак предстательной железы. (A, B) Поперечные и продольные картины серошкального ТРУЗИ, изображающие локальный узелок в правой периферической зоне (стрелки в А и В). (С, D) Увеличение васкуляризации было обнаружено в поражении на поперечных и продольных изображениях энергетического допплеровского ТРУЗИ (стрелки C и D).

Рис. 5. Рак предстательной железы. (А) Изображение в поперечной проекции серошкального ТРУЗИ показывает диффузно неоднородную паренхиматозную эхотекстуру с неравномерным контуром капсулы и заметным задним экстракапсулярным распространением. Поражение имеет заметное выпячивание и близость к стенке прямой кишки, что подразумевает инфильтрацию раковой ткани. Поперечное цветное (B) и энергетическое (С) допплеровское ТРУЗИ изображения выявляют увеличенное кровоснабжение пораженного участка. (D) Сцинтиграфия всего тела того же пациента показывает несколько областей повышенного поглощения в осевом скелете, что представляет патологическую активность остеобластов и соответствует метастатическому поражению.
Маленькие раковые опухоли, как правило, имеют гипоэхогенный вид, в то время как увеличение опухоли может привести к трансформации в изоэхогенное поражение или в образование с неоднородным эхосигналом. Не существует специфических ультразвуковых характеристик для переходных зон рака, хотя они отличаются от периферической зоны рака тем, что они являются менее агрессивными клинически. Следовательно, рутинная биопсия является единственным средством для обнаружения переходной зоны рака. Наличие сопутствующей ДГПЖ может быть ограничивающим фактором при ТРУЗИ оценке предстательной железы, потому что его смешанный отраженный сигнал или эффект компрессии периферической зоны может маскировать РПЖ.
Помимо аденокарциномы, которая является наиболее часто встречающимся гистологическим типом РПЖ, ультразвуковые особенности редких опухолей предстательной железы также описаны. Аденоматозная кистозная карцинома предстательной железы может проявляться с несколькими однородными небольшими кистами. Комедокарцинома, будучи наиболее злокачественной формой PП, появляется сонографически как раковая гипоэхогенная зона, которая перемежается с неоднородными многочисленными небольшими гиперэхогенными очагами. Лимфома, с другой стороны, имеет ультразвуковую картину больших гипоэхогенных образований в переходной и периферической зонах. В заключение, мягкотканные образования, которые проникают в мочевой пузырь и предстательную железу могут представлять картину рабдомиосаркомы - злокачественной опухоли, которая развивается в детстве.
Хотя использование ТРУЗИ и ограничено для постановки диагноза РПЖ, некоторые выводы ТРУЗИ могут выявлять экстракапсулярное распространение. Среди этих выводов: локальное выпячивание или неравномерность капсулы предстательной железы и гипоэхогенные полосы в плоскости перипростатической жировой ткани. Однако, ТРУЗИ не может выявлять экстракапсулярное распространение малых микроскопических кластеров опухолевых клеток.
Допплерография является средством для оценки местного кровотока, который тесно связан с функцией ткани и ее жизнеспособностью. При цветной допплерографии, цветная палитра связана с направлением потока крови и ориентацией датчика при приеме сигнала, где поток к датчику изображается в оттенках красного, а поток от датчика в оттенках синего. С другой стороны, увеличение потребности в кровоснабжении раковой ткани с ускоренным темпом роста более выражено, чем в нормальной ткани, что может привести к значительным изменениям в показателях местной гемодинамики. Как следствие это влияет на способность визуализации и обнаружения раковых образований при цветной допплерографии (рис. 5B). В опухолевой ткани увеличение числа расширенных и нетипичных кровеносных сосудов, которые отражают ангиогенез и увеличение кровотока, может быть обнаружено при цветной допплерографии (рис. 2 В). Технически, увеличение кровотока может быть показано либо при спектральном анализе при импульсно-волновой допплерографии путем выявления волн, представляющие сдвиг частоты или скорости, либо цветной допплерографии, при которой изображается спектр цветов, представляющих средний диапазон сдвига частоты или скорости эритроцитов в кровотоке.
Ранее считалось, что цветная допплерография обеспечивает лучшую диагностику РПЖ, так как она позволяла определить диффузный, локальный и окружающий характер кровотока. Позже выяснилось, что специфичность техники для соответствующей оценки была низкой. Кроме того, было также отмечено, что гипоэхогенное поражение, которое подразумевает РПЖ и гиперваскуляризация, не обязательно коррелируют (рис. 3B, C). Тем не менее, было показано, что цветной допплеровский сигнал имеет хорошую корреляцию со стадией и типом РПЖ, а также с риском рецидива после лечения, что является ключом к определению поведения и агрессивности РПЖ. Соответственно, цветная допплерография была полезна в дифференциальной диагностике гиповаскулярных опухолей низкого риска от гиперваскулярных опухолей высокого риска, так как последняя группа связана с гиперваскуляризацией, что представляет более высокий уровень опухолевой стадии по классификации Глисона, что подразумевает более высокий риск экстрапростатического распространения опухоли (рис. 5). Прицельная биопсия, которая зависит исключительно от высокочастотного цветного или энергетического допплеровского изображения, не рекомендуется из-за теоретического риска пропуска значительного количества опухолей. Кроме количественной оценки кровотока, с помощью цветной допплерографии можно провести расчет плотности микрососудов (распределение микрососудов), что может быть полезным для оценки кровотока в предстательной железе. Естественно, что увеличенная плотность микрососудов была выше в метастатических опухолях, что является типичным для РПЖ. Из-за того, что кор-биопсия может недооценивать гистологическую картину, соответствующую шкале Глисона, плотность микрососудов может быть использована в качестве индикатора прогноза заболевания. Среди технических ограничений цветной допплерографии для оценки предстательной железы являются: угловая зависимость допплеровского потока, интрапростатический шум, имитирующий усиление кровотока и неадекватность методики обнаружения при низких скоростях кровотока.
Энергетическая допплерография имеет меньшую угловую зависимость, чем цветная допплерография и предоставляет информацию о наличии и интенсивности сигналов потока. Техника имеет преимущество в обнаружении медленного потока и даже незначительных изменений кровотока в мелких опухолевых сосудах (рис. 4 и 5). Тем не менее, направление потока не может быть оценено с помощью этого метода. Энергетическая допплерография, которая имеет от 3 до 4-кратной чувствительность для обнаружения РПЖ, также помогает в дифференциальной диагностике ДГПЖ и РПЖ. Тем не менее, об этом методе редко сообщается информация о каком-либо преимуществе перед цветной допплерографией в обнаружении РПЖ. Хотя энергетическая допплерография и может помочь в определении необходимого места для биопсии предстательной железы путем выявления области локальной гиперваскуляризации, считается, что эта методика не превосходит цветную допплерографию и только может быть полезной для прицельной биопсии в том случае, когда количество биопсийных пункций через железу ограничено. Биопсия под комбинированным ультразвуковым наведением серошкальной сонографии и цветной допплерографии при ТРУЗИ не является достаточно чувствительной для того, чтобы исключить необходимость в рутинной биопсии. В недавнем исследовании было опубликовано, что спектральное измерение формы сигнала капсулярных и уретральных артерий предстательной железы при энергетической допплерографии может быть полезно в дифференциальной диагностике РПЖ от доброкачественной гипертрофии. Исследователи также предполагают, что увеличение числа биоптатов на границе с аномальными значениями спектрального допплеровского индекса повысит диагностическую ценность в выявлении РПЖ.
Микропузырьки - контрастные вещества, которые позволяют визуализировать микрососудистое русло предстательной железы, что может улучшить обнаружение РПЖ, потому что повышенная плотность микрососудов, которая ассоциируется с ангионеогенезом в раковой ткани предстательной железы меньше, чем уровень разрешающей способности обычной допплерографии. В тоже время, большинство ультразвуковых контрастных веществ с диаметром менее 10 мкм имеют способность проникать даже в самые мелкие кровеносные сосуды. В связи с этим, ультразвуковое исследование с контрастным усилением (УИКУ) позволяет оператору получить изображение контрастных веществ в виде микропузырьков. Таким образом, несоответствие между акустическими свойствами микропузырьков и окружающей кровью приводит к интенсификации отражений ультразвуковой волны.
Примерно через 20 секунд после внутривенного введения, число ультразвуковых эхосигналов увеличивается в сосудистом русле предстательной железы и это обеспечивает улучшение допплеровского сдвигового сигнала, что усиливает чувствительность измерений цветной и энергетической допплерографии. Максимальное контрастностное усиление развивается приблизительно от 1 до 2 минут после однократного внутривенного болюсного введения, хотя время усиления может быть расширено путем внутривенной инфузии микропузырьков. Время пикового усиления, в то же время, показывает часть предстательной железы с раковым поражением.
В целом, УИКУ улучшает чувствительность в обнаружении РПЖ без снижения специфичности исследования. УИКУ может также способствовать снижению количества попыток отбора проб, что обеспечивает прицельную биопсию. С другой стороны, 3-мерная энергетическая допплерография, с контрастным усилением с 3-мерной реконструкцией изображения до и после введения контрастных веществ, и уровни ПСА считаются оптимальной прогностической комбинацией для диагностики РПЖ. Тем не менее, основным недостатком для клинического использования энергетической и цветной допплерографии с контрастным усилением является то, что кровоток при этом методе в основном определяется в крупных сосудах, потому что микропузырьки разрушаются при допплерографии до достижения опухолевых неососудов.
Серошкальное гармоническое ультразвуковое исследование является еще одним способом для визуализации микропузырьковых контрастных агентов. Метод предполагает использование более низких энергий для изображения контрастных веществ с меньшим разрушением пузырьков и, соответственно, большим их проникновением в микрососуды. В отличие от цветной допплерографии с контрастным усилением, гармонические методы визуализации включают обнаружение нелинейных эхосигналов пузырьков. Технология фазовой инверсии (инверсия импульса), с помощью изображения с широкой пропускной способностью, улучшает оценку тканевой перфузии в связи с лучшим обнаружением сигналов, отраженных от микропузырьков. Кроме того, изображения с высоким разрешением, которые воспроизводятся этой техникой, в отличие от традиционной ультразвуковой технологии, с узкой полосой пропускания, что приводит к потере пространственного разрешения. Серошкальное гармоническое ультразвуковое исследование может повысить чувствительность обнаружения РПЖ. Кроме того, более высокая степень усиления, как уже было показано, связана с более высокой степенью по шкале Глисона. Недавно был разработан метод перемежающейся визуализации, который обеспечивает более длительный срок персистирования микропузырьковых контрастных агентов. По сравнению с непрерывным гармоническим исследованием, метод перемежающей гармонической визуализации обеспечивает лучшее усиление паренхимы. В последнее время было отмечено, что техника флэш наполнения в отличие от гармонической методики улучшает прицельность зон с повышенной микрососудистой васкуляризацией при биопсии предстательной железы под ТРУЗИ наведением. В недавнем исследовании, которое проводилось после премедикации дутастерида (двойной ингибитор 5а редуктазы) до биопсии предстательной железы, был продемонстрирован ограниченный кровоток в доброкачественной ткани предстательной железы, в отличие от раковой ткани. Совсем недавно контраст-модулированная последовательная импульсная технология улучшила визуализацию микрососудов, которые связанны с РПЖ и, таким образом, улучшилась частота обнаружения РПЖ.
В общем, УИКУ улучшает визуализацию РПЖ благодаря развитию новых специфических ультразвуковых методов и лучшей визуализации микрососудов, которые ассоциируются с РПЖ, хотя чувствительность и специфичность до сих пор остается не достаточно высокой для того, чтобы избежать рутинной биопсии. Хотя прицельная биопсия вместе с рутинным отбором проб согласно протоколам, увеличивает частоту обнаружения патологии, роль УИКУ в рутинной клинической практике остается дискутабельной.
Эластография включает оценку эластичности исследуемых тканей. Технически, отраженные ультразвуковые сигналы незначительно изменяются в разной степени, если исследуемая ткань слегка сжимается и затем разжимается во время исследования. Сжимаемость исследуемой ткани изменяется во времени или пространстве между зонами исследования с различными коэффициентами сжатия. Специально разработанный ТРУЗИ датчик необходим для применения метода при визуализации предстательной железы. Технически, небольшие изменения в давлении датчиком, который прикладывается к предстательной железе при ТРУЗИ исследовании, приводят к изменениям в создаваемом изображении в режиме реального времени и визуализируют только изменения в локальной компрессии тканей. Соответственно, может быть проведена дифференциальная диагностика между раковыми и доброкачественными тканями, в зависимости от градиента плотности и снижения степени эластичности. РПЖ, который характеризуется ограниченной упругостью или сжимаемостью, изображается сонографически как темная зона. Следовательно, это исследование можно считать потенциальным методом визуализации для обнаружения РПЖ. Хотя использование эластографии при ТРУЗИ исследовании помогает увеличить выявляемость РПЖ по маркировке мест для биопсии, данная методика пока не может исключить потребность в рутинной биопсии предстательной железы. Также было отмечено, что данная техника потенциально эффективна в улучшении точности определения стадии процесса при ТРУЗИ.
Процедура биопсии предстательной железы резко изменилась благодаря достижениям в области технологии ТРУЗИ. Было решено, что биопсия предстательной железы под ТРУЗИ наведением является золотым стандартом для обнаружения РПЖ. Комбинированное использование ТРУЗИ и игольной биопсии позволило направлять биопсийную иглу именно в область поражения, что в результате привело к увеличению возможности обнаружения РПЖ в сравнении с биопсией под контролем пальца (рис. 3D). Кроме того, биопсия предстательной железы играет ключевую роль в лечении РПЖ. Показания для проведения биопсии предстательной железы под ТРУЗИ наведением:
Классически, изменения при пальцевом ректальном исследовании, повышенный уровень ОПСА (> 4 нг/мл) и подозрительные признаки при ТРУЗИ исследовании являются основными показаниями для проведения биопсии предстательной железы под ТРУЗИ наведением, хотя до сих пор не существует консенсуса по верхнему пределу нормального значения ПСА. Процедура основана на региональном рутинном отборе проб ткани из зон предстательной железы, где по данным исследования, скорее всего, расположена опухоль. Но так как данная патология имеет многоцентровой характер, индивидуальная диагностическая способность ТРУЗИ в обнаружении рака ограничена. В зависимости от дизайна датчика, отбор проб ткани предстательной железы выполняется либо при сагиттальном, либо при аксиальном сканировании. Выстрел из биопсийного пистолета должен быть выполнен только после идентификации капсулы предстательной железы с помощью биопсийной иглы для того, чтобы избежать контаминации перипростатическими тканями, и как можно больше ткани включить в образец пробы. Кроме того, длина траектории иглы в пределах железы должна быть просчитана с помощью линии-траектории на ультразвуковом экране, таким образом случайное проникновение в структуры, такие как: мочеиспускательный канал и перипростатическая ткань, может быть предотвращено.
Так как РПЖ преимущественно возникает в периферической зоне и агрессивность рака периферической зоны выше, чем в переходной зоне, отбор проб для биопсии должен быть сосредоточен на периферической зоне. Протокол классической шеститочечной биопсии включает образцы ткани из точки посредине между боковой границей и срединной плоскостью на уровне основания, средней части железы и верхушки железы, соответственно. Был разработан также развернутый протокол отбора проб для биопсии, который включает от 10 до 12 образцов ткани с участием дополнительных боковых участков ткани на указанных уровнях, хотя все еще существуют споры в отношении оптимальных зон и количества биопсий. Как сообщалось, увеличение объема предстательной железы имеет негативное влияние на диагностический результат, при таком же количестве участков ткани. В настоящее время при выполнении первичной биопсии не выполняется отбор проб из внутренней части железы из-за низкой выявляемости рака и метастатического потенциала поражения внутренней части железы. Посредством биопсии предстательной железы под ТРУЗИ наведением также может быть определена стадия по шкале Глисона, как оценка агрессивности РПЖ.
Для того, чтобы свести к минимуму риск инфицирования, связанный с процедурой, рекомендуется антибиотикопрофилактику ципрофлоксацином начинать за день до процедуры и продолжать в течение 3 следующих дней. Кроме того, применение очищающих ректальных клизм рассматривается как мера профилактики против инфекционных осложнений и, что очень важно, в получении хорошего ТРУЗИ изображения. В недавнем исследовании сообщалось, что пациенты с уретральным катетером, с сахарным диабетом, или те, кто подвергался биопсии из более, чем 10 зон железы, должны быть подвергнуты наблюдению после биопсии предстательной железы, потому что они имеют больший риск развития инфекции мочевыводящих путей.
Из-за растущего внимания к облегчению дискомфорта пациента во время биопсии предстательной железы под ТРУЗИ наведением, в последнее время стало популярным применение нескольких методов обезболивания. Среди них перипростатическая блокада нервов под ультразвуковым наведением была наиболее эффективным методом, который применяется большинством врачей. После проникновения под фасцию Данонвилье, на уровне задней полуокружности основания предстательной железы с использованием иглы 22 номера, анестезирующее вещество (лидокаин без адреналина) вводится латерально возле белого пирамидального участка между предстательной железой и семенными пузырьками, который также называют признак «горы Эверест» в связи с его белым, остроконечным внешним видом из-за жировой ткани в этой зоне при сагиттальном сканировании. Постепенно появляется ультразвуковая картина скопления жидкости в виде гипоэхогенного заполнения зоны «горы Эверест». Однако, все еще существует спор в отношении точного места инъекции, количества и дозы препаратов. Более важно то, что введение анестетика предпочтительно осуществляют в период до процедуры для того, чтобы обеспечить достаточное время наступления эффекта. Данная методика может иметь некоторые нежелательные эффекты, такие как: боль, вызванная проколом иглой, которая используется для местной анестезии, необходимость повторных инъекций в течение процедуры биопсии, рутинная токсичность лидокаина, недержание мочи, искажение или образование артефактов на ТРУЗИ изображениях, перипростатическая инфекция и эректильная дисфункция. Кроме того, оператор-зависимый характер и неэффективность техники в присутствии факторов риска, таких как: беспокойство пациента, молодой возраст, повторная биопсия или воспалительные заболевания анального канала существуют также среди недостатков данного метода, при этом седация с внутривенным введением мидазолама является альтернативным и эффективным средством анестезии.
Радикальная простатэктомия (РПЭ) является эффективным средством лечения клинически локализованного РПЖ. После РПЭ, рецидивирующий РПЖ является важной клинической проблемой в долгосрочной перспективе приблизительно у 40% пациентов, при этом более чем 95% рецидивов происходит в первые 5 лет. Не удивительно, что более раннее обнаружение местного рецидива рака может позволить пациентам начать местную лучевую терапию в потенциально более курабельной стадии заболевания. Хорошо известно, что уровень ПСА должен быть меньше, чем 0,4 нг/мл в течение от 2 до 3 недель после РПЭ. В связи с этим, повышение уровня ПСА предполагает местный рецидив РПЖ в области ямки предстательной железы, метастатическое поражение или сочетание и того, и другого. В этой связи, ПСА уровень является самым полезным маркером опухоли для мониторинга пациентов с рецидивом РПЖ после РПЭ. Клинически, диагноз местного рецидива РПЖ основывается на комбинированном использовании пальцевого ректального исследования, ТРУЗИ и биопсии предстательной железы под ТРУЗИ наведением. В целом, ТРУЗИ считается эффективной процедурой, потому что это позволяет провести точную оценку анатомии нормальной и патологически измененной ямки предстательной железы. У пациентов без клинических или биохимических признаков местного рецидива после РПЭ, ТРУЗИ, как правило, отображает внешний вид щелевидного конического профиля, простирающийся от шейки мочевого пузыря до везикоуретрального анастомоза, который окружен переменным количеством гипоэхогенной ткани. В частности, гипоэхогенная зона вблизи везикоуретрального анастомоза, шейки мочевого пузыря или позади треугольника Льето считается патологической, хотя асимметричное утолщение везикоуретрального анастомоза или отсутствие целостности ретроанастомотической плоскости жировой ткани также следует рассматривать, как подозрительные зоны для местного рецидива (рис. 6А, В).
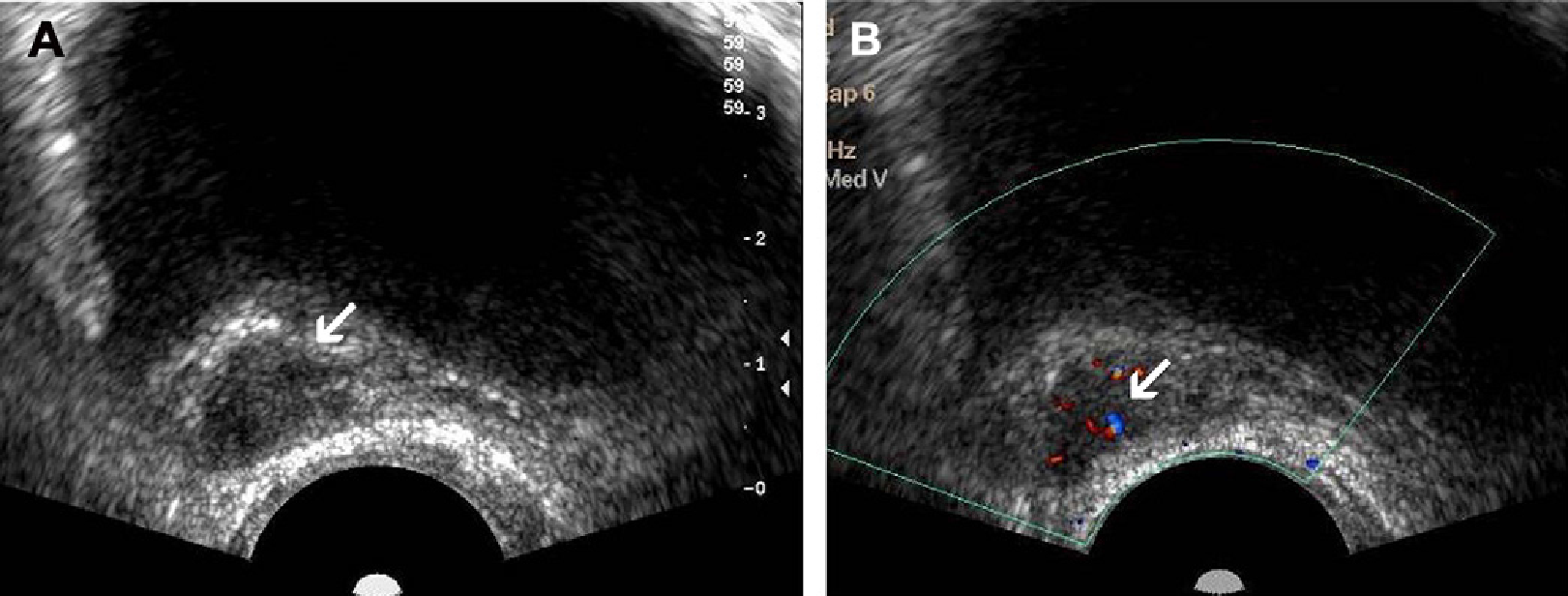
Рис. 6. Местный рецидив после радикальной простатэктомии. (А) Изображение в поперечной проекции серошкального ТРУЗИ, которое показывает нечетко определяемое, гипоэхогенное образование в ямке предстательной железы, которая прилегает к области анастомоза (стрелка), которая позже гистопатологически оказалась рецидивирующей аденокарциномой. (В) Изображение поперечного цветного допплеровского ТРУЗИ, на котором в очаге поражения выявлены области повышенной васкуляризации, что связано с неоваскуляризацией опухоли (стрелка).
Тем не менее, серошкальное ТРУЗИ не может исключить необходимость в биопсии ямки предстательной железы под ТРУЗИ наведением для дифференциальной диагностики между послеоперационным фиброзом и рецидивом РПЖ. С другой стороны, энергетическое допплеровское ТРУЗИ, которое облегчает идентификацию гиперваскуляризированных зон в пределах опухолевой ткани во время биопсии предстательной железы под ТРУЗИ наведением, считается эффективным для раннего выявления локальных рецидивов опухоли.
ДГПЖ является распространенным заболеванием среди пожилых мужчин, которая включает в себя узловую гиперплазию фиброзной, мышечной и железистой ткани в пределах периуретральной железистой зоны и переходной зоны. Основная роль ультрасонографии при исследовании пациентов с ДГПЖ является в оценке размера предстательной железы и объема остаточной мочи (ООМ) до лечения. Методика также может быть использована для оценки объема переходной зоны, которая тесно связана с тяжестью ДГПЖ. Трансабдоминальное ультразвуковое исследование может играть роль при последующем динамическом наблюдении за пациентами с ДГПЖ, потому что оно эффективно в расчете повышения уровня ООМ. Повышение уровня ООМ увеличивает риск задержки мочи. Кроме того, верхние мочевыводящие пути также должны быть исследованы на предмет любых изменений.
Основные ТРУЗИ изменения при ДГПЖ – диффузное или узловое увеличение переходной зоны с гипоэхогенным или гетерогенным проявлением, в сравнении с периферической зоной, выпячивание капсулы предстательной железы, кистозные изменения и кальцификаты в аденоматозных узелках и компрессия периферической зоны, увеличенной переходной зоной. Кроме того, могут быть обнаружены соответствующие изменения в проксимальных отделах мочевыводящих путей, таких как: подъем основания мочевого пузыря, увеличение ООМ, образование трабекул мочевого пузыря и гидроуретеронефроза, которые являются вторичными по отношению к той или иной степени инфравезикальной непроходимости. Хирургический дефект может быть обнаружен в центральной части переходной зоны у пациентов с предшествующей трансуретральной резекцией предстательной железы в связи с ДГПЖ, который не должен быть неверно истолкован как кистозное поражение. Кисты, вторичные по отношению к дегенерации гиперпластических узелков, связанных с ДГПЖ, достаточно распространены в клинической практике. Самое главное, выпячивание увеличенной переходной зоны не следует путать с опухолями, которые развиваются из основы мочевого пузыря. Точная дифференциальная диагностика может быть проведена путем выявления прерывания контура поражения и предстательной железы при сагиттальном ТРУЗИ сканировании.
Термин простатит используется для разнообразных нарушений предстательной железы, которые вызывают боль в области таза и в основном имеющие небактериальную этиологию. Клинически данная патология классифицируется как острый бактериальный простатит, хронический бактериальный простатит, хронический асептический простатит, синдром хронической тазовой боли и асимптоматический простатит. Роль ТРУЗИ ограничена у больных с острым простатитом, потому что диагноз в основном базируется на клинической картине. Пациенты с острым простатитом обычно жалуются на лихорадку, боль, дизурические расстройства, эмпирические позывы и пиурию, и даже выражают значительный дискомфорт при введении датчика в прямую кишку из-за сильной боли воспаленной предстательной железы. При ТРУЗИ могут быть видны такие воспалительные изменения, как округлая, увеличенная предстательная железа с уменьшенной эхогенностью и диффузной гиперваскуляризацией при цветной или энергетической допплерографии. Тем не менее, основная роль ТРУЗИ при остром простатите – исключить формирование абсцесса у больных, которые не реагируют на лечение.
Абсцесс предстательной железы, который развивается в основном на пятом или шестом десятилетии жизни - редкое осложнение острого бактериального простатита. Типичная ТРУЗИ картина – хорошо определяемая, толстостенная, одно- или многокамерное жидкостное образование с внутренним эхосигналом и перегородками, которое в основном расположено в переходной зоне (рис. 7А).
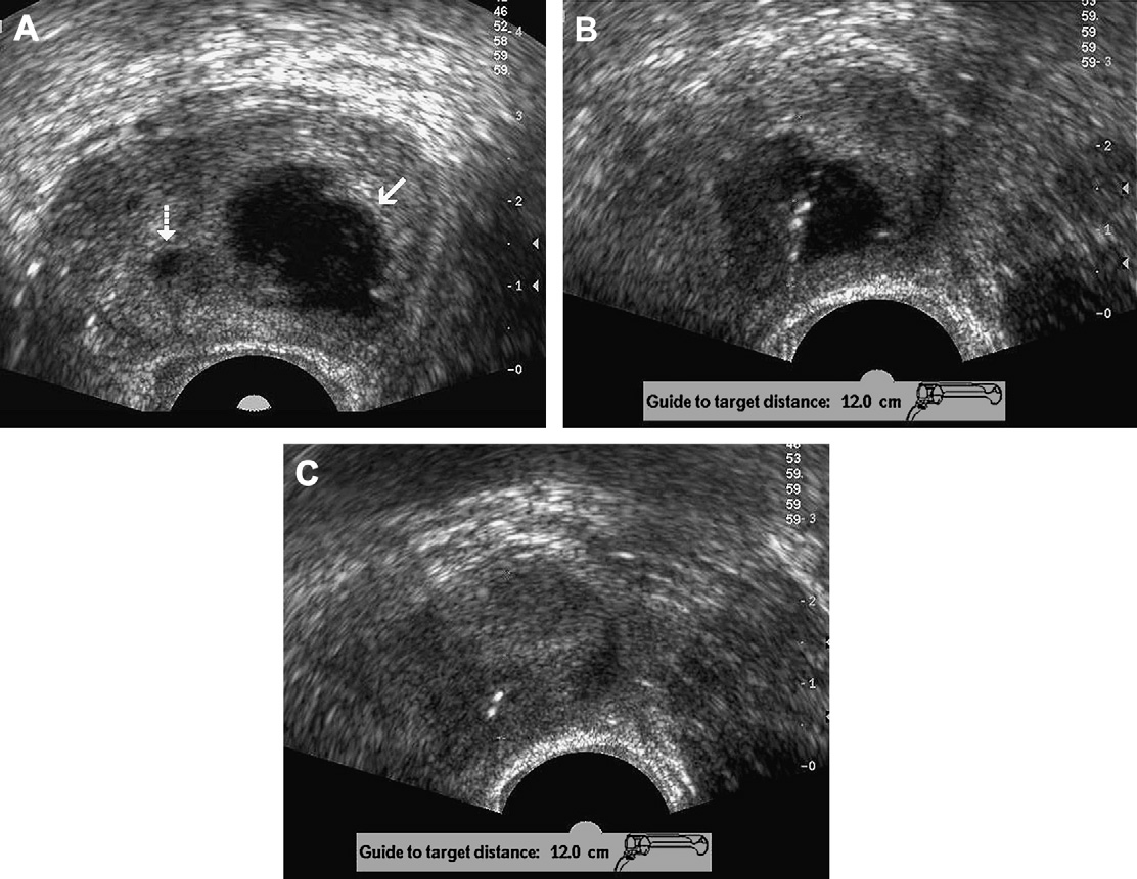
Рис. 7. Абсцесс предстательной железы. (А) Картина поперечной проекции серошкального ТРУЗИ, которая показывает полость большого абсцесса в левой внутренней части железы с внутренним эхосигналом (стрелки), с дополнительным меньшим жидкостным скоплением в правой внутренней части железы. (В) Было выполнено внешнее дренирование очага поражения в левой внутренней части железы под ультразвуковым наведением. (С) ТРУЗИ также может быть использовано для оценки эффективности интервенционного лечения вышеупомянутого абсцесса.
Помимо проведения оценки морфологических особенностей абсцесса, ТРУЗИ также обеспечивает ультразвуковое наведение для дренирования поражения (рис. 7В). В связи с этим, дренирование рекомендуется для абсцесса больше, чем 1,5 см в диаметре, в то время как лечение антибиотиками является предпочтительным для абсцессов меньшего размера. Последующее динамическое наблюдение для определения эффективности, либо характера лечения, также может быть выполнено с помощью ТРУЗИ (рис. 7С).
Хронический простатит, как правило, представлен неспецифическими симптомами нижних мочевыводящих путей, что проявляется сонографически как пятнистое, гипоэхогенное поражение или участками с гетерогенной, или повышенной эхогенностью (рис. 8А). Увеличение кровоснабжения вышеупомянутого поражения при цветной допплерографии, дистрофическая кальцификация, неравномерность и утолщение капсулы, дилатация перипростатических вен и неравномерность околомочеточниковой зоны - также могут быть обнаружены у пациентов с хроническим простатитом (рис. 8B).

Рис. 8. Хронический простатит. (А) Картина поперечной проекции серошкального ТРУЗИ, выявляет гетерогенную эхотекстуру паренхимы с гипоэхогенными областями, имеющими неоднородное распределение. (В) Поперечная проекция энергетической допплерографии при ТРУЗИ того же пациента показывает увеличение васкуляризации всей ткани железы. Рутинная биопсия под ТРУЗИ наведением гистопатологически показала хронический простатит.
Редко простатит может быть вовлечен в гранулематозный процесс, что приводит к увеличению предстательной железы с локальными или мультифокальными гипоэхогенными поражениями (рис. 9A-C).

Рис. 9. Гранулематозный простатит. (A-C) Картина в поперечной и продольной проекции серошкального ТРУЗИ, показывает увеличенную предстательную железу с гетерогенной эхотекстурой паренхимы с несколькими, случайно распределенными, гипоэхогенными поражениями. Цветная допплерография показывает повышенную васкуляризацию. ТРУЗИ биопсия гистопатологически выявила гранулематозный простатит.
Туберкулез является наиболее распространенным типом инфекционного гранулематозного простатита, который, как правило, развивается вторично при прохождении мочи через простатическую часть мочеиспускательного канала. Сопутствующее вовлечение эякуляторных протоков может привести к образованию стриктур. Из-за отсутствия конкретных признаков при ТРУЗИ, биопсия является единственным средством для постановки правильного диагноза.
Маточковые кисты и кисты Мюллерова протока - наиболее характерные срединные кисты предстательной железы, которые вряд ли могут быть отдифференцированы по клиническим данным или с помощью методов визуализации. Они могут быть бессимптомными или редко провоцировать клинику обструктивной уропатии или бесплодия. Кисты Мюллерова протока, которые, как правило больше, чем маточковые кисты, расположены немного сбоку средней линии и часто имеют супрапростатическое расширение. Маточковые кисты обычно ассоциируются с такими аномалиями, как гипоспадии, крипторхизм или почечная агенезия, и могут быть диагностированы у мужчин более младшего возраста. Крайне редко, РПЖ может быть обнаружен при обоих типах кист. Кистозные полости, которые расположены по средней линии и сзади от уретры являются типичной находкой, хотя гипоэхогенный внутренний инфекционный дебрис также может быть обнаружен.
Менее характерные кисты эякуляционного протока, которые развиваются вторично по отношению к обструкции эякуляторных протоков либо врожденные, либо вторичные к воспалительным процессам. Сонографически они проявляются, как округлой или овальной формы, тонкостенные, однокамерные кистозные поражения с парасрединной локализацией. Крайне редко они могут вызвать одностороннее расширение семенного пузырька.
Комментариев еще нет
Если вы впервые на сайте, заполните, пожалуйста, регистрационную форму.
Балацкая Марина Викторовна
Редакция Ultrasound Club
Погодин Дмитрий Юрьевич
Морозов Александр Иванович
Базилова Зейнеп Рахимбаевна
Кабанов Владимир Анатольевич
Мишин Валерий Петрович
Садиров Талгат Сабитович
Макаров Артем Владимирович