Tadashi Sekimotoa, Hitoshi Maruyamaa,а, Takayuki Kondo a, Taro Shimada a, Masanori Takahashi a, Osamu Yokosukaa, Masayuki Otsuka b, Masaru Miyazaki b, Yoshitaka Mine c
а – отделение медицины и клинической онкологии, медицинский университет Чиба, Япония
б – отделение общей хирургии, медицинский университет Чиба, Япония
с – Toshiba Medical Systems Corporation, отделение ультразвуковых систем, отделение развития ультразвуковых систем, Япония
Ключевые слова: цирроз, печень, ультразвук, трехмерная визуализация, лапароскопия, 3Д, Fly Thru
Цель: изучить потенциальную эффективность 3D-реконструированных сонограмм в дифференциальной диагностике печени с цирротическими изменениями, путем визуализации особенностей поверхности печени.
Материалы и методы: было проведено предварительное исследование на фантоме с целью изучения возможного разрешения 3D-изображений, распознавания неровностей поверхности, как разницу её высоты. В проспективном клиническом исследовании 31 пациента с асцитом (21 с циррозом, 10 – без цирроза), были получены данные об объемах печени путем трансабдоминального механического сканирования. Особенности поверхности печени пациентов с циррозом и без цирроза сравнивались 2 независимыми экспертами. Также было изучено внутри- и межисследовательское согласование.
Результаты: Исследование фантома показало, что показатель в 0.4 мм был минимальной узнаваемой разницей в высоте на 3D сонограммах. Изображение поверхности печени было успешно получено у 74% пациентов (23/31). Успех зависел от количества асцитической жидкости; визуализация была у 100% пациентов с асцитом 10 мм или более между печеночной поверхностью и передней брюшной стенкой. Изображения показали неравномерность печеночной поверхности у всех пациентов с циррозом. Внешний вид поверхности печени был расценен как очень похожий у 3 пациентов, которые имели как 3D-ультразвуковое исследование, так и резекцию печени для трансплантации. Способность различать цирроз печени от печени без цирроза был усовершенствован с использованием комбинации 2D- и 3D-визуализации, по сравнению с одними только 2D-изображениями (чувствительность – р = 0,02; точность – p = 0,02) или 3D-визуализацией самостоятельно (чувствительность – р = 0.03). Получено отличное внутри- и межисследовательское согласование (к = 1,0).
Вывод: 3D сонографическая визуализация печеночной поверхности показала высокую надежность и воспроизводимость, может использоватся в качестве метода виртуальной лапароскопии. Данная техника имеет большой потенциал для улучшения качества диагностики цирроза печени.
Цирроз печени связан с широким спектром этиологических факторов и является последней стадии заболевания печени. Это имеет серьезные последствия для пациентов, так как приводит к гепатоцеллюлярной карциноме, портальной гипертензии и печеночной недостаточности. Учитывая поступательное прогрессирования заболевания печени, начиная с хронического гепатита, диагноз цирроза печени должен быть точно поставлен для того, чтобы обеспечить надлежащее лечение заболеванием.
Биопсия печени остается золотым стандартом оценки степени фиброза печени. Тем не менее, выполнение биопсии может быть проблематичным в таких случаях, так как она является инвазивным методом, а это особенно опасно для пациентов с нарушением коагуляции из-за прогрессирующего заболевания печени. Кроме того, методика склонна к возможной ошибке выборки из-за гетерогенно распределенного фиброза печени.
В последнее десятилетие, различные исследователи пытались определить стадию заболевания печени с использованием неинвазивных маркеров, некоторые из которых показали существенную корреляцию со степенью фиброза печени. Однако, морфологические особенности печени непосредственно отражают стадию заболевания печени, и, следовательно, лапароскопия является полезным инструментом для диагностики заболеваний печени. Прямая диагностическая лапароскопия редко выполняется из-за его инвазивности. Тем не менее, анализ печеночной структуры поверхности дает полезную информацию для классификации и характеристики заболеваний печени.
Мы предположили, что спроецированное изображение, созданное из трансабдоминальных сонографических объемных данных, полученных с помощью исследования гипоэхогенной зоны (асцит), позволит визуализировать поверхность печеночной структуры. Целью данного исследования было изучить потенциальную эффективность 3-мерных (3D) реконструированных сонограмм для различия между цирротической и нецирротической печенью, на основе внешнего вида печеночной поверхности.
2.1. Пациенты
Это проспективное исследование было одобрено этическим комитетом больницы университета Чиба и выполнено в период с августа 2011 года по апрель 2012 года. Пациенты с асцитом были потенциальными кандидатами для данного исследования, поскольку наличие асцита может обеспечить виртуальную отметку для оценки особенностей печеночной поверхности на сонограммах. Они были отобраны из пациентов с асцитом, обнаруженных с помощью ультразвукового исследования (УЗД) во время плановых осмотров в нашем отделении. Пациенты были исключены из исследования, если они: (I) имели очаговые поражения печени на сонограммах, или (II) не могли задерживать дыхание в течение нескольких секунд.
2.2. Ультразвуковая Система
Aplio 500 ультразвуковая система (Toshiba, Токио, Япония) была использована для работы с изображениями. Сканирование в правом межреберье было выполнено для всех пациентов для получения изображений в положении лежа на спине. Сначала выбиралась лучшая позиция для сканирования с помощью обычного 2-мерного (2D) УЗД, а затем измерялось расстояние между брюшной стенкой и печеночной поверхностью, как показатель количества асцитической жидкости. Затем настройка изменялась для 3D визуализации (Fly Thru режим, Toshiba, Токио, Япония). Мы использовали PVT675MV (6,0 МГц), специализированный датчик для 3D сканирования, с механической системой сканирования автоматической развертки. Область интереса была установлена таким образом, чтобы захватить поверхность печени, а центр фокуса был установлен на средней глубине между самым поверхностным и самым глубоким уровнем поверхности. Объемные 3D изображения были получены путем автоматического сканирования с максимальным углом обзора 75◦. До получения изображения, пациенты были проинструктированы задерживать дыхание в течение примерно 4-6 секунд. Полученные объемные изображения были сразу же сохранены на жесткий диск ультразвуковой системы.
Оператор исследования HM – гепатолог с более, чем 20-летним опытом работы в ультразвуковой диагностике, и TS – гепатолог с более, чем 6-летним опыт работы в ультразвуковой диагностике. Три комплекта 3D изображения были получены для каждого пациента у каждого оператора.
2.3. Эксперимент с фантомом и его оценка
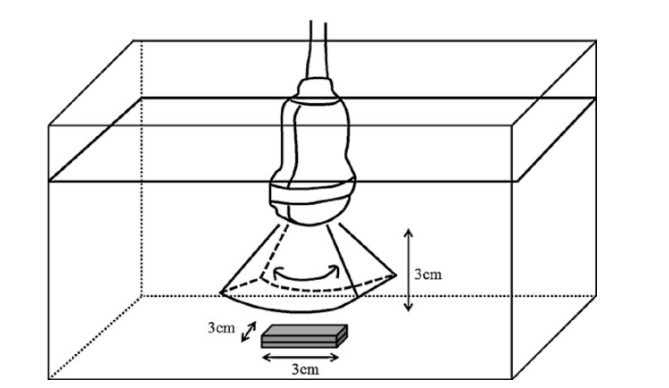
Данный эксперимент был проведен с целью изучения возможностей разрешения реконструированных 3D изображений в распознавании различия высоты в каждом изображении (рис. 1). Одна или несколько пластиковых пластин (площадью 9 см2, толщиной 0,2 мм) были размещены на дне бака, заполненного водой: 1 пластина – 0.2 мм высотой, 2 пластины – 0.4 мм высотой, 3 пластины – 0.6 мм высотой, 4 пластины – 0,8 мм высотой, и 5 пластин – 1.0 мм высотой. Датчик был также помещен в резервуар с водой для получения 3D-изображение над пластиковыми пластинами, с такими же настройками аппарата, которые используются у пациентов. Расстояние между датчиком и пластиной было 3 см. Три эксперта оценивали реконструированные изображения, с целью определения наличия различий в высоте.
2.4. Объективная оценка характеристики печеночной поверхности
Для каждого пациента, были выбраны 2 репрезентативных изображения которые, показывали внешний вид поверхности печени; 1 из 2D-изображений, а другое из 3D реконструированных изображений. Отбор осуществляется оператором (HM) для слепой оценки данных печеночной поверхности. Два эксперта (TS и OY) ставили диагноз цирроза/отсутствие цирроза на основании 2D или 3D сонограмм.
Результаты оценки поверхности печени на 2D-изображениях оценивались по трем признакам: ровная поверхность, шероховатая поверхность или неровная поверхность. Цирроз диагностировался при наличии неровной поверхности, а отсутствие цирроза на основании диагноз ровной/ шероховатой поверхности. В то же время, на 3D-изображения, были применены следующие две категории: (I) ровная поверхность, шероховатая поверхность или узловая картина при характеристике поверхности, (II) частичное или диффузное распределение признаков при характеристике поверхности. Цирроз диагностировался при узловой картине и диффузном распределении, а отсутствие цирроза при других характеристиках. Затем оценивали диагностическую эффективность 2D-, 3D- и сочетание 2D и 3D визуализации.
После этого, были оценены внутри- и межисследовательские согласования с использованием 4 изображений: 1 пара изображений (группа А), полученная тем же оператором и 1 пара изображений (группа В), полученная другими операторами. Отбор проводился HM для того, чтобы обеспечить репрезентативными изображения с точки зрения угла зрения, яркости и контрастности. Если бы было больше, чем два изображения, которые были адекватными для обзора, два из них выбирались случайным образом. Эти согласования были оценены двумя рецензентами (TS и OY), которые не имели информации о пациенте. Каждый из них выбирал пары изображений независимо друг от друга, из группы А для внутриисследовательского согласования и из группы B для межисследовательского согласования. Если пары изображений были отобраны правильно, то это оценивалось как положительное согласование.
Рис. 1. Схема для эксперимента на фантоме. Одна или несколько пластиковых пластин (площадью 9 см2, толщиной 0,2 мм) были размещены на дне бака, заполненного водой: 1 пластина – 0.2 мм высотой, 2 пластины – 0.4 мм высотой, 3 пластины – 0.6 мм высотой, 4 пластины – 0,8 мм высотой, и 5 пластин – 1.0 мм высотой. Датчик был также помещен в резервуар с водой для получения 3D-изображение над пластиковыми пластинами, с такими же настройками аппарата, которые используются у пациентов. Расстояние между датчиком и пластиной было 3 см.
2.5. Статистический анализ
Все данные представлены как среднее значение ± стандартное отклонение (SD) или в процентах. Чувствительность, специфичность и точность диагностики цирроза печени были получены с помощью формул: истинно положительный/(истинно положительный + ложно отрицательный результат), истинный отрицательный/(ложно положительный + истинно отрицательный) и (истинно положительный + истинно отрицательный)/общее число, соответственно. Внутриисследовательское согласование и меж-/внутриисследовательское согласование были оценены путем расчета kappa значения. Степени согласования был определены как <0,2 для плохого, 0,2-0,4 для умеренного, 0,4-0,6 достаточного, 0,6-0,8 для хорошего и 0,8-1,0 для отлично. Статистическую значимость определяли с помощью теста хи-квадрат с порогом р <0,05. Статистический анализ проводили с использованием программного обеспечения SPSS (версия 13.0J; SPSS Inc., Чикаго, Иллинойс, США).
3.1. Эксперимент с фантомом
Все 3 эксперта пришли к выводу, что реконструированные 3D сонограммы поверхностей, полученные с помощью Fly Thru, наглядно отображали разницу в высоте на изображениях при высоте 0.4мм (таблица 1, рис. 2).
Таблица 1
Рис. 2. Эксперимент на фантоме для определения потенциального разрешение 3D-реконструированных сонограмм для распознавания разницы в высоте на изображении с пластиковыми пластинами. (А) Одна пластина для высоты 0.2мм. (В) 2 пластины для высоты 0.4мм. (С) 3 пластины для высоты 0.6мм. (D) 4 пластины для высоты 0.8мм. (Е) 5 пластин для высоты 1.0мм. Все 3 рецензенты пришли к выводу, что 3D-реконструированные изображения поверхности, полученные при помощи Fly Thru, наглядно продемонстрировали разницу в высоте на изображениях с высотой 0.4мм.
3.2. Характеристики пациентов
В исследование включено 31 пациент с асцитом, 21 пациент с циррозом (возрастной диапазон – 41-81 лет, среднее ± стандартное отклонение – 60±11; 15 мужчин и 6 женщин) и 10 пациентов без цирроза (возрастной диапазон – 28- 81 год, среднее ± стандартное отклонение – 65±14; 9 мужчин и 1 женщина). Цирроз был диагностирован как в результате анализа изображений, так и биохимических результатов, у 17 пациентов с использованием образцов, полученных с помощью трансюгулярной игольной биопсии, или во время трансплантации – у 4 больных. Этиология цирроза была следующая: гепатит В – 3 случаях, вирус гепатита С – в 14 случаях, злоупотребление алкоголем – в 2-х случаях и криптогенная – в 2-х случаях. Причины асцита у 10 пациентов без цирроза были: карциноматозный перитонит в 3-х случаях, тяжелая гипоальбуминемии вследствие болезни Crow Fukase – в 1 случае, первичный билиарный цирроз печени (Шойера II по данным биопсии печени) – в 1 случае, идиопатическая тромбоцитопеническая пурпура – в 1, застойная печень – в 1, неходжкинская лимфома – в 1 случае и неизвестная патология – в 2-х случаях. У этих 10 пациентов был исключен цирроз на основании как визуализации, так и биохимических исследований. Все субъекты в исследовании имели трансудативный асцит, а расстояние между брюшной стенкой и печеночной поверхностью из-за асцита было 2-50 мм (21±14), как было определено по сонограммам, полученных при сканировании в правом межреберье.
3.3. Изображения поверхности печени
3D-реконструкция печеночной поверхности была успешно произведена у 74% пациентов (23/31); 71% (15/21) пациентов с циррозом и 80% (8/10) больных без цирроза. Успех зависел от количества асцитической жидкости. 100% визуализация была достигнута у пациентов с асцитом более 10 мм между печеночной поверхностью и передней брюшной стенкой. Изображения печени показали отчетливые нарушения печеночной поверхности у всех пациентов с циррозом (рис. 3). Внешний вид поверхности печени был расценен как очень похожий у 3 пациентов, которым выполнена 3D сонография до трансплантации печени, затем проведена резекции для трансплантации (рис. 4).
Рис. 3. Изображения поверхности печени по 3D-реконструированным объемным данным. (А) Печень без цирроза. 68-летняя женщина с карциноматозным перитонитом. Изображение показывает гладкую поверхность. (В) Цирротическая печень. 49-летняя женщина с гепатитом C с исходом в цирроз печени. Изображение показало видимую неровность поверхности печени с узловатой картиной.
///
Обсуждение
Диагностирование цирроза печени остается сложной задачей для врачей, несмотря на появление различных неинвазивных маркеров. Насколько нам известно, это первое исследование, которое сообщает об успешной демонстрации особенностей печеночных поверхностей с помощью неинвазивного метода визуализации. Оба признака: неровность печеночной поверхности и округлые края четко визуализируются на 3D сонограммах, данная техника обладает высоким разрешением, надежностью и воспроизводимостью. Этот механизм визуализации представляет собой «виртуальную лапароскопию» для постановки точного диагноза цирроза печени.
В заключение, мы показали возможность использования 3D-сонограмм для визуализации печеночных поверхностных структур с достаточной степенью надежности и воспроизводимости. Это доступный и неинвазивный метод визуализации “Fly Thru”, который имеет высокий визуальный потенциал, служит в качестве метода виртуальной лапароскопии и может в значительной степени влиять на диагностику цирроза печени.
Комментариев еще нет
Если вы впервые на сайте, заполните, пожалуйста, регистрационную форму.
1 1 1